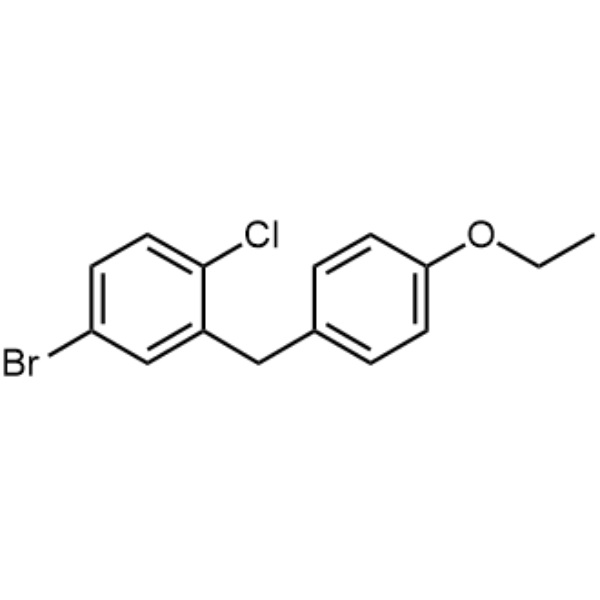
5-Bromo-2-Cloro-4′-Etossidifenilmetano CAS 461432-23-5 Dapagliflozin intermedio
Fornitura del produttore, elevata purezza, produzione commerciale
Dapagliflozin (CAS: 461432-26-8) Intermedi correlati:
5-Bromo-2-Acido clorobenzoico CAS 21739-92-4
5-Bromo-2-Cloro-4'-Etossidifenilmetano CAS 461432-23-5
2,3,4,6-Tetrakis-O-Trimetilsilil-D-Gluconolattone CAS 32384-65-9
| Nome chimico | 5-Bromo-2-Cloro-4'-Etossidifenilmetano |
| Sinonimi | 4-Bromo-1-Cloro-2-(4-Etossibenzil)benzene; 4-(5-Brom-2-Clorobenzil)fenil-Etere etilico; Dapagliflozin bromo impurità |
| Numero CAS | 461432-23-5 |
| Stato delle scorte | Disponibile, la produzione scala fino a tonnellate |
| Formula molecolare | C15H14BrClO |
| Peso Molecolare | 325,63 |
| Punto di fusione | Da 41,0 a 43,0 ℃ |
| Densità | 1,371±0,06 g/cm3 |
| Certificato di autenticità e scheda di sicurezza | Disponibile |
| Luogo d'origine | Shangai, Cina |
| Marchio | Ruifu chimica |
| Articolo | Specifiche | Risultati |
| Aspetto | Polvere cristallina da bianca a giallo pallido | Conforme |
| Metodo di purezza/analisi | ≥98,0% (HPLC) | 98,91% |
| Acqua (K.F) | ≤0,50% | 0,15% |
| Spettro infrarosso | Conforme alla struttura | Conforme |
| Spettro 1H NMR | Conforme alla struttura | Conforme |
| Prova standard | Standard aziendale | Conforme |
| Applicazione | Intermedio di Dapagliflozin (CAS: 461432-26-8), diabete di tipo II | |
Pacchetto: Bottiglia, sacchetto di foglio di alluminio, fusto di cartone, 25 kg/fusto, o secondo le esigenze del cliente.
Condizioni di conservazione:Conservare in contenitori sigillati in luogo fresco e asciutto; Proteggere dalla luce e dall'umidità.

4-Bromo-1-Cloro-2-(4-Ethoxybenzyl)benzene (CAS: 461432-23-5) è utilizzato come intermedio nella sintesi di Dapagliflozin (CAS: 461432-26-8). Dapagliflozin è un potente inibitore selettivo del cotrasportatore renale sodio-dipendente del glucosio 2 (SGLT2) per il trattamento del diabete di tipo 2. Dapagliflozin è un nuovo farmaco antidiabetico sviluppato congiuntamente da Bristol-Myers Squibb e AstraZeneca, approvato dall'Agenzia europea per i medicinali (EMA) il 12 novembre 2012. L'8 gennaio 2014, la Food and Drug Administration (FDA) statunitense ne ha approvato l'uso nel trattamento del diabete di tipo II.