Acyclovir CAS 59277-89-3 Test 98,0-101,0% (HPLC) API Factory Antivirale Alta qualità
Shanghai Ruifu Chemical Co., Ltd. è il produttore leader di Aciclovir (CAS: 59277-89-3) con API di alta qualità, utilizzato per trattare le infezioni da HSV e VZV. Ruifu Chemical fornisce intermedi farmaceutici e API da oltre 15 anni. Ruifu Chemical può fornire consegne in tutto il mondo, prezzi competitivi e un servizio eccellente.
Acquista Acyclovir o altri prodotti, si prega di inviare un'e-mail a: alvin@ruifuchem.com
| Nome chimico | Aciclovir |
| Sinonimi | ACV; Acicloguanosina; 9-[(2-Idrossietossi)metil]guanina; Aciclovir |
| Numero CAS | 59277-89-3 |
| Stato delle scorte | Disponibile, la produzione arriva fino a centinaia di chilogrammi |
| Formula molecolare | C8H11N5O3 |
| Peso Molecolare | 225.2 |
| Punto di fusione | 256,0~257,0℃ |
| Certificato di autenticità e scheda di sicurezza | Disponibile |
| Origine del prodotto | Shangai, Cina |
| Categorie di prodotti | API (ingrediente farmaceutico attivo) |
| Marchio | Ruifu chimica |
| Articolo | Specifiche | Risultati |
| Aspetto | Polvere cristallina bianca | Conforme |
| Assorbimento degli infrarossi | Positivo | Conforme |
| Tempo di ritenzione (HPLC) | Positivo | Conforme |
| Contenuto d'acqua (di KF) | ≤6,00% | 5,20% |
| Impurezze Ordinarie (TLC) | ≤1,00% | <1,00% |
| Limite per la guanina (HPLC) | ≤0,70% | 0,18% |
| Metalli pesanti | ≤20 ppm | Conforme |
| Metodo di analisi/test | 98,0%-101,0% (Calcolato su base anidra) | 99,20% |
| Conclusione | Il prodotto è stato testato ed è conforme allo standard USP35. | |
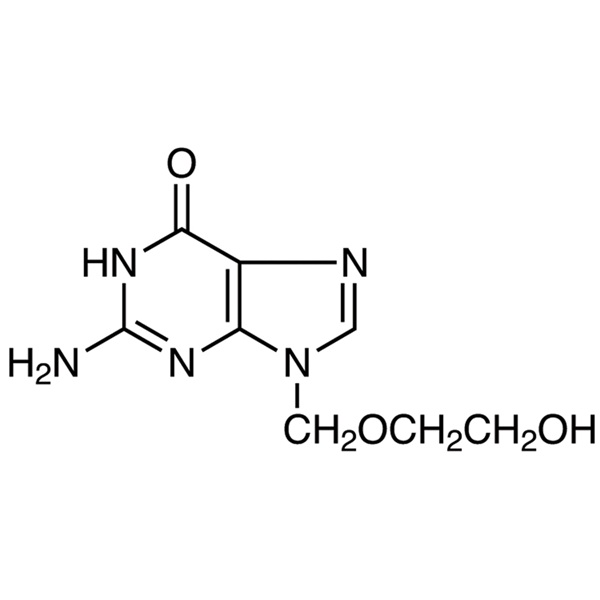
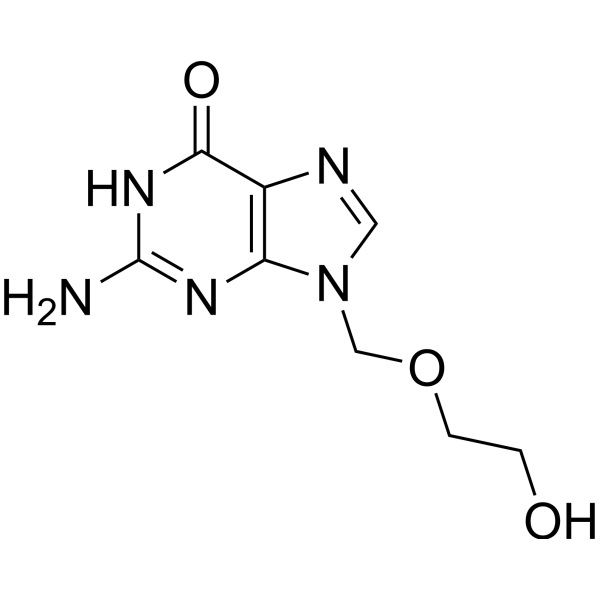
Aciclovir
C8H11N5O3 225,20
6H-Purina-6-one, 2-ammino-1,9-diidro-9-[(2-idrossietossi)metil]-.
9-[(2-Idrossietossi)metil]guanina [59277-89-3].
» L'aciclovir contiene non meno del 98,0% e non più del 101,0% di C8H11N5O3, calcolato su base anidra.
Imballaggio e stoccaggio- Conservare in contenitori stretti. Conservare a temperatura ambiente. Proteggere dalla luce e dall'umidità.
Norme di riferimento USP<11>-
USP Aciclovir RS -
Identificazione-
A: Assorbimento degli infrarossi <197K>.
B: Il tempo di ritenzione del picco principale nel cromatogramma della preparazione del dosaggio corrisponde a quello nel cromatogramma della preparazione dello standard, come ottenuto nel dosaggio e al limite per la guanina.
Acqua, Metodo I<921>: non più del 6,0%.
Impurezze ordinarie<466>-
Soluzione di prova: dimetilsolfossido.
Soluzione standard: dimetilsolfossido.
Eluente: una miscela di cloroformio, metanolo e idrossido di ammonio (80:20:2).
Visualizzazione: 1.
Volume di applicazione: 5 µl.
Limite: 1%.
Dosaggio e limite per la guanina-
Fase mobile- Preparare una soluzione filtrata e degasata di acido acetico glaciale in acqua (1 su 1000). Se necessario, apportare le modifiche (vedere Idoneità del sistema in Cromatografia<621>).
Soluzione di idoneità del sistema 1- Sciogliere quantità accuratamente pesate di USP Acyclovir RS e guanina in idrossido di sodio 0,1 N e diluire quantitativamente, e gradualmente se necessario, con acqua per ottenere una soluzione con concentrazioni note di circa 0,1 mg di ciascuno per mL.
Soluzione di idoneità del sistema 2- Sciogliere una quantità accuratamente pesata di guanina in idrossido di sodio 0,1 N e diluire quantitativamente, e gradualmente se necessario, con acqua per ottenere una soluzione avente una concentrazione nota di circa 0,7 µg per mL.
Preparazione standard della guanina- Trasferire circa 8,75 mg di guanina, accuratamente pesati, in un matraccio tarato da 500-mL. Sciogliere in 50 mL di idrossido di sodio 0,1 N, diluire con acqua a volume e mescolare. Trasferire 2,0 mL di questa soluzione in un matraccio tarato da 50-mL, diluire con idrossido di sodio 0,01 N a volume e mescolare per ottenere una soluzione avente una concentrazione di circa 0,7 µg per mL.
Preparazione standard- Sciogliere circa 25 mg di USP Acyclovir RS, accuratamente pesati, in 5 mL di idrossido di sodio 0,1 N in un matraccio tarato da 50-mL, diluire con acqua a volume e mescolare. Trasferire 10,0 mL di questa soluzione in un matraccio tarato da 50-mL, diluire con idrossido di sodio 0,01 N a volume e mescolare per ottenere una soluzione avente una concentrazione nota di circa 0,1 mg di Aciclovir RS USP per mL.
Preparazione del test- Sciogliere circa 100 mg di Aciclovir, accuratamente pesati, in 20 mL di idrossido di sodio 0,1 N in un matraccio tarato da 200-mL, diluire con acqua a volume e mescolare. Trasferire 10,0 mL di questa soluzione in un matraccio tarato da 50-mL, diluire con idrossido di sodio 0,01 N fino al volume e mescolare.
Sistema cromatografico (vedi Cromatografia<621>)- Il cromatografo liquido è dotato di un rilevatore da 254-nm e di una colonna da 4,6-mm × 25-cm che contiene l'impaccamento L1. La portata è di circa 3 ml al minuto. Soluzione 1 di idoneità del sistema cromatografico e registrare le risposte di picco come indicato nella Procedura: la risoluzione, R, tra aciclovir e guanina non è inferiore a 2,0; il fattore di scodamento per il picco dell'analita non è superiore a 2; e la deviazione standard relativa per le iniezioni ripetute per il picco dell'aciclovir non è superiore al 2,0%. Soluzione 2 di idoneità del sistema cromatografico e registrare le risposte di picco come indicato nella Procedura: la deviazione standard relativa per le iniezioni replicate non è superiore al 2,0%.
Procedura- Iniettare separatamente volumi uguali (circa 20 µl) della preparazione standard, della preparazione standard della guanina e della preparazione del test nel cromatografo, registrare i cromatogrammi e misurare le risposte per tutti i picchi. Calcolare la quantità, in µg, di guanina nella porzione di Aciclovir assunta con la formula:
1000°C(rU/rS)
in cui C è la concentrazione, in µg per mL, di guanina nella preparazione standard di Guanina; e rU e rS sono le risposte di picco dovute alla guanina rispettivamente nella preparazione del test e nella preparazione dello standard della guanina: non viene trovato più dello 0,7% di guanina. Calcolare la quantità, in mg, di C8H11N5O3 nella porzione di Aciclovir assunta con la formula:
1000°C(rU/rS)
in cui C è la concentrazione, in mg per ml, di USP Acyclovir RS nella preparazione Standard; e rU e rS sono le risposte di picco dovute all'aciclovir rispettivamente nella preparazione del test e nella preparazione dello standard.
Pacchetto: Bottiglia, sacchetto di alluminio, fusto da 25 kg/cartone o secondo le esigenze del cliente.
Condizioni di conservazione: Tenere il contenitore ben chiuso e conservarlo in un magazzino fresco, asciutto e ben ventilato, lontano da sostanze incompatibili. Tenere lontano dalla luce del sole; evitare fuoco e fonti di calore; evitare l'umidità.
Spedizione: Consegna in tutto il mondo via aerea, tramite FedEx / DHL Express. Fornire consegne rapide e affidabili.

Codici di rischio R36/37/38 - Irritante per gli occhi, le vie respiratorie e la pelle.
R40- Prove limitate di un effetto cancerogeno
R20/21/22 - Nocivo per inalazione, contatto con la pelle e per ingestione.
Descrizione di sicurezza S22 - Non respirare la polvere.
S24/25 - Evitare il contatto con la pelle e gli occhi.
S36 - Indossare indumenti protettivi idonei.
S26 - In caso di contatto con gli occhi, lavare immediatamente e abbondantemente con acqua e consultare un medico.
S23 - Non respirare i vapori.
WGK Germania 2
RTECS UP0791400
Codice HS 2933990099
Classe di pericolo IRRITANTE
L'aciclovir (ACV, CAS 59277-89-3), noto anche come acicloguanosina, è un farmaco antivirale. Viene utilizzato principalmente per il trattamento delle infezioni da herpes simplex, varicella e fuoco di Sant'Antonio. Altri usi includono la prevenzione delle infezioni da citomegalovirus dopo il trapianto e le gravi complicanze dell'infezione da virus Epstein-Barr. Può essere assunto per via orale, applicato come crema o iniettato. L'aciclovir è usato per trattare le infezioni da HSV e VZV. L'aciclovir è un analogo purinico sintetico derivato dalla guanina. Esercita i suoi effetti sul virus dell'herpes simplex (HSV) e sul virus varicella-zoster interferendo con la sintesi del DNA attraverso la fosforilazione da parte della timidina chinasi virale e la successiva inibizione della DNA polimerasi virale, inibendo così la replicazione virale. L'aciclovir è stato brevettato nel 1974 e approvato per uso medico nel 1981. È presente nell'elenco dei medicinali essenziali dell'Organizzazione mondiale della sanità. È disponibile come farmaco generico ed è commercializzato con molti marchi in tutto il mondo.