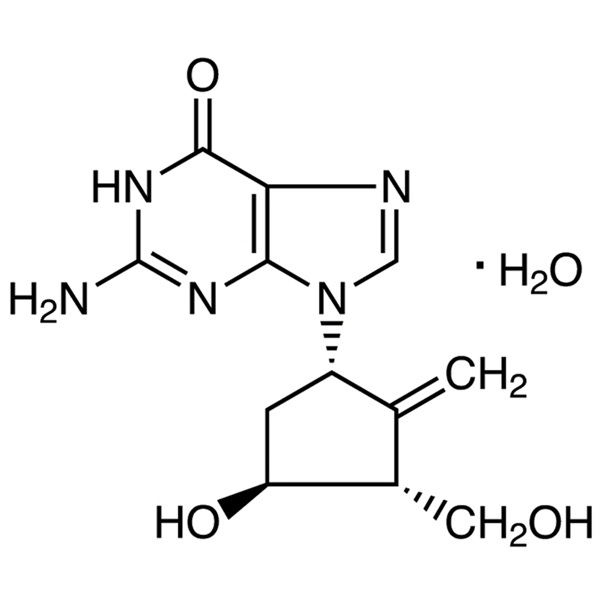
Entecavir monoidrato CAS 209216-23-9 Analisi 98,0%~102,0% API USP EP Infezione antivirale standard per epatite B
Ruifu Chemical è il fornitore leader di Entecavir monoidrato (CAS: 209216-23-9) di alta qualità, in grado di soddisfare gli standard USP/EP, utilizzato nel trattamento dell'infezione da epatite B.
Ruifu fornisce API e intermedi farmaceutici da oltre 15 anni.
Ruifu Chemical può fornire consegne in tutto il mondo, prezzi competitivi e un servizio eccellente.
Acquista Entecavir monoidrato, vi preghiamo di contattarci via e-mail: alvin@ruifuchem.com
| Nome chimico | Entecavir monoidrato |
| Sinonimi | Entecavir Idrato; 9-[(1S,3R,4S)-4-Idrossi-3-(idrossimetil)-2-metilenciclopentil]guanina monoidrato |
| Numero CAS | 209216-23-9 |
| Stato delle scorte | Disponibile, la produzione scala fino a tonnellate |
| Formula molecolare | C12H17N5O4 |
| Peso Molecolare | 295.3 |
| Punto di fusione | >220℃ |
| Densità | 1.81 |
| Condizioni di spedizione | Spedito a temperatura ambiente |
| Certificato di autenticità e scheda di sicurezza | Disponibile |
| Origine del prodotto | Shangai, Cina |
| Categorie di prodotti | API (ingrediente farmaceutico attivo) |
| Marchio | Ruifu chimica |
| Articolo | Specifiche |
| Aspetto | Polvere cristallina bianca o quasi bianca |
| Solubilità | Liberamente solubile in dimetilformammide, leggermente solubile in acqua, etanolo e metanolo |
| IR di identificazione | Lo spettro del campione corrisponde a quello dello standard di riferimento |
| Identificazione HPLC | Il tempo di ritenzione del campione in esame corrisponde a quello dello standard di riferimento |
| Contenuto d'acqua (di KF) | 5,5%~6,5% |
| Rotazione ottica specifica | da +24,0° a +30,0° (DMF: MeOH=1:1 C=1%) (su sostanza anidra) |
| Residuo all'accensione | ≤0,10% |
| Sostanze correlate | |
| Furoentecavir | ≤0,10% |
| Entecavir 1-Epimero | ≤0,10% |
| Entecavir 3-Epimero | ≤0,10% |
| 8-Idrossi-Entecavir | ≤0,10% |
| Entecavir 4-Epimero | ≤0,10% |
| 8-Metossi Entecavir | ≤0,10% |
| 4-Dimetilsilil Entecavir | ≤0,10% |
| Composto correlato a Entecavir A | ≤0,10% |
| Qualsiasi impurità non specificata | ≤0,10% |
| Impurità totali | ≤0,30% |
| Solventi residui | |
| Metanolo | ≤600 ppm |
| Diclorometano | ≤300 ppm |
| Acetato di etile | ≤1000 ppm |
| Tetraidrofurano | ≤720 ppm |
| Toluene | ≤890 ppm |
| Cloruro di benzile | ≤1000 ppm |
| Alcool benzilico | ≤1000 ppm |
| Limite microbico | |
| Conteggi aerobici totali | ≤100ufc/g |
| Lieviti e Muffe | ≤10ufc/g |
| Escherichia Coli | Non dovrebbe essere rilevato |
| Metalli pesanti | ≤10 ppm |
| Analisi | 98,0%~102,0% (HPLC; su base anidra) |
| Dimensione delle particelle | Il 95% delle particelle dovrebbe trovarsi entro 125μm |
| Prova standard | Standard aziendale; Standard della farmacopea degli Stati Uniti (USP). |
| Utilizzo | Farmaco antivirale utilizzato nel trattamento dell'infezione da epatite B |
Pacchetto: Bottiglia, sacchetto di alluminio, fusto da 25 kg/cartone o secondo le esigenze del cliente.
Condizioni di conservazione: Tenere il contenitore ben chiuso. Conservare in un magazzino fresco, asciutto (2-15℃) e ben ventilato, lontano da sostanze incompatibili. Tenere lontano dalla luce del sole; evitare fuoco e fonti di calore; evitare l'umidità.
Spedizione: Consegna in tutto il mondo via aerea, via mare, tramite FedEx / DHL Express. Fornire consegne rapide e affidabili.

| Descrizione di sicurezza | 24/25- Evitare il contatto con la pelle e gli occhi. |
| Codice SA | 2933990099 |
Entecavir monoidrato (CAS 209216-23-9) è un farmaco antivirale orale utilizzato nel trattamento dell'infezione da virus dell'epatite B (HBV). Entecavir monoidrato è un analogo nucleosidico (più specificamente, un analogo della guanina) che inibisce la trascrizione inversa, la replicazione del DNA e la trascrizione nel vira. Si tratta di un nuovo tipo di farmaco ciclopentilacilguanosina anti-virus dell'epatite B con effetti farmacologici simili a quelli di Entecavir. Viene applicato clinicamente al trattamento dell'epatite B cronica negli adulti in cui vi è replicazione virale attiva, aumento delle transaminasi sieriche ALT o lesioni attive evidenziate dall'istologia epatica. Entecavir monoidrato è un inibitore potente e selettivo dell'HBV, con un EC50 di 3,75 nM nelle cellule HepG2. Entecavir è un inibitore della trascrittasi inversa. Impedisce al virus dell'epatite B (HBV) di moltiplicarsi e riduce la quantità di virus nel corpo.
Entecavir
C12H15N5O3·H2O 295,29
6H-Purin-6-one, 2-ammino-1,9-diidro-9-[(1S,3R,4S)-4-idrossi-3-(idrossimetil)-2-metilenciclopentile]-, monoidrato;
9-[(1S,3R,4S)-4-Idrossi-3-(idrossimetil)-2-metilenciclopentil]guanina monoidrato [209216-23-9]; UNII:5968Y6H45M.
Anidro 277,28
DEFINIZIONE
Entecavir è un monoidrato e contiene NLT 98% e NMT 102% di Entecavir (C12H15N5O3), calcolato su base anidra.
IDENTIFICAZIONE
Cambia in:
• A. TEST DI IDENTIFICAZIONE SPETTROSCOPICA<197>, Spettroscopia infrarossa: 197A o 197K (CN 1-Maggio-2020)
• B. Il tempo di ritenzione del picco maggiore della soluzione campione corrisponde a quello della soluzione standard, come ottenuto nel test.
SAGGIO
• PROCEDURA
Soluzione A: acetonitrile e acqua (3:97)
Soluzione B: acetonitrile
Fase mobile: vedere la Tabella 1. [NOTA- I tempi di eluizione del gradiente vengono stabiliti su un sistema HPLC con un volume di permanenza di circa 1,0 ml.]
Tabella 1 Tempo (min) Soluzione A (%) Soluzione B (%)
0 100 0
8 100 0
50 77 23
75 17 83
90 100 0
100 100 0
Soluzione madre di idoneità del sistema: 1,0 mg/mL di miscela RS di idoneità del sistema USP Entecavir in metanolo
Soluzione di idoneità del sistema: 0,2 mg/mL di miscela RS di idoneità del sistema USP Entecavir nella soluzione A dalla soluzione madre di idoneità del sistema
Soluzione madre standard: 1,0 mg/ml di USP Entecavir Monoidrato RS in metanolo. Sonicare secondo necessità.
Soluzione standard: 0,2 mg/mL di USP Entecavir Monoidrato RS nella soluzione A dalla soluzione madre standard
Soluzione madre del campione: 1,0 mg/mL di Entecavir in metanolo. Sonicare secondo necessità.
Soluzione campione: 0,2 mg/ml di Entecavir nella soluzione A dalla soluzione madre del campione
Sistema cromatografico
(Vedere Cromatografia<621>, Idoneità del sistema.)
Modalità:LC
Rivelatore: UV 254 nm
Colonna: 4,6-mm × 25-cm; 5-μm imballaggio L1
Velocità di flusso: 1 ml/min
Volume di iniezione: 10 µl
Idoneità del sistema
Esempi: soluzione di idoneità del sistema e soluzione standard
[NOTA- Vedere la Tabella 2 per i relativi tempi di ritenzione dei componenti nella soluzione di idoneità del sistema.]
Requisiti di idoneità
Risoluzione: NLT 3,5 tra entecavir 1-epimero ed entecavir; NLT 2.0 tra entecavir e 8-idrossi entecavir, Sistema
soluzione di idoneità
Fattore di scodamento: 0,8-1,5 per entecavir, soluzione di idoneità del sistema
Deviazione standard relativa: NMT 1,5%, Soluzione standard
Analisi
Campioni: soluzione standard e soluzione campione
Calcolare la percentuale di entecavir (C12H15N5O3) nella porzione di Entecavir assunta:
Risultato = (ru /rs ) × (Cs /Cu ) × 100
ru = risposta di picco di entecavir dalla soluzione campione
rs = risposta di picco di entecavir dalla soluzione Standard
Cs = concentrazione di USP Entecavir Monoidrato RS nella soluzione standard (mg/mL)
Cu = concentrazione di Entecavir nella soluzione campione (mg/mL)
Criteri di accettazione: 98%-102% su base anidra
IMPURITÀ
• IMPURITÀ ORGANICHE
Soluzione A, Soluzione B, Fase mobile, Soluzione madre di idoneità del sistema, Soluzione madre di idoneità del sistema, Soluzione madre del campione, Soluzione del campione e Sistema cromatografico: procedere come indicato nel dosaggio.
Soluzione madre standard: utilizzare la soluzione standard del dosaggio.
Soluzione standard: 0,2 µg/mL di USP Entecavir Monoidrato RS nella soluzione A dalla soluzione madre standard
Idoneità del sistema
Esempi: soluzione di idoneità del sistema e soluzione standard
[NOTA- Vedere la Tabella 2 per i tempi di ritenzione relativi dei componenti nella soluzione di idoneità del sistema.]
Requisiti di idoneità
Risoluzione: NLT 3,5 tra entecavir 1-epimero ed entecavir; NLT 2.0 tra entecavir e 8-idrossi entecavir, soluzione di idoneità del sistema
Fattore di scodamento: 0,8-1,5 per entecavir, soluzione di idoneità del sistema
Deviazione standard relativa: NMT 10,0%, Soluzione standard
Analisi
Campioni: soluzione campione e soluzione standard
Calcolare la percentuale di ciascuna impurezza nella porzione di Entecavir assunta:
Risultato = (ru /rs ) × (Cs /Cu ) × (1/F) × 100
ru = risposta di picco di ciascuna impurità dalla soluzione campione
rs = risposta di picco di entecavir dalla soluzione Standard
Cs = concentrazione di USP Entecavir Monoidrato RS nella soluzione standard (mg/mL)
Cu = concentrazione di Entecavir nella soluzione campione (mg/mL)
F = fattore di risposta relativo (vedi Tabella 2)
Criteri di accettazione: vedere la Tabella 2. Ignorare qualsiasi picco inferiore allo 0,05%.
Tabella 2
Nome Tempo di ritenzione relativo Fattore di risposta relativo Criteri di accettazione, NMT (%)
Furoentecavir a 0,73 1,0 0,1
Entecavir 1-epimero b 0,93 1,0 0,1
Entecavir 3-epimero c 0,96 1,0 0,1
Entecavir 1.0 - -
8-Idrossi entecavir d 1,03 0,67 0,1
Entecavir 4-epimero e 1,08 1,0 0,1
8-Metossi entecavir f 1,27 0,67 0,1
4-Dimetilsilil entecavir g 1,84 1,0 0,1
Composto A 3.41 correlato a entecavir - -
Qualsiasi impurità non specificata - 1,0 0,1
Impurità totali i - - 0,3
a 9-[(3aS,4S,6S,6aR)-3a,6-Diidrossiesaidro-1H-ciclopenta[c]furano-4-il]guanina.
b 9-[(1R,3R,4S)-4-Idrossi-3-(idrossimetil)-2-metilenciclopentil]guanina.
c 9-[(1S,3S,4S)-4-Idrossi-3-(idrossimetil)-2-metilenciclopentil]guanina.
d 8-idrossi-9-[(1S,3R,4S)-4-idrossi-3-(idrossimetil)-2-metilenciclopentil]guanina.
e 9-[(1S,3R,4R)-4-Idrossi-3-(idrossimetil)-2-metilenciclopentil]guanina.
f 8-metossi-9-[(1S,3R,4S)-4-idrossi-3-(idrossimetil)-2-metilenciclopentil]guanina.
g 9-[(1S,3R,4S)-4-idrossidimetilsilil-3-(idrossimetil)-2-metilenciclopentil]guanina.
hSolo a titolo informativo; quantificato nel test per il limite del composto A correlato a Entecavir.
i Include la somma di tutte le impurità rilevate nei test per il limite del composto A correlato a Entecavir e le impurità organiche.
• LIMITE DEL COMPOSTO CORRELATO A ENTECAVIR A
Soluzione A: acido trifluoroacetico allo 0,1% (v/v) in acqua
Soluzione B: acido trifluoroacetico allo 0,1% (v/v) in acetonitrile
Fase mobile: vedere la tabella 3. [NOTA- I tempi di eluizione del gradiente vengono stabiliti su un sistema HPLC con un volume di permanenza di
circa 1,0 ml.]
Tabella 3
Tempo (min) Soluzione A (%) Soluzione B (%)
0 65 35
8 53 47
8,1 65 35
11 65 35
Soluzione standard: 2 µg/mL di composto A RS correlato a Entecavir USP in metanolo
Soluzione campione: 1,0 mg/mL di Entecavir in metanolo. Sonicare secondo necessità.
Sistema cromatografico
(Vedere Cromatografia<621>, Idoneità del sistema.)
Modalità:LC
Rivelatore: UV 254 nm
Colonna: 4,6-mm × 5-cm; 5-μm imballaggio L1
Temperature
Campionatore automatico: 4°
Colonna: 30°
Velocità di flusso: 2 ml/min
Volume di iniezione: 10 µl
Idoneità del sistema
Campione: soluzione standard
Requisiti di idoneità
Fattore di scodamento: 0,8-1,5
Deviazione standard relativa: NMT 3,0%
Analisi
Campioni: soluzione standard e soluzione campione
Calcolare la percentuale del composto A correlato a entecavir nella porzione di Entecavir assunta:
Risultato = (ru /rs ) × (Cs /Cu ) × 100
ru = risposta di picco del composto A correlato a entecavir dalla soluzione campione
rs = risposta di picco del composto A correlato a entecavir dalla soluzione standard
Cs = concentrazione del composto A RS correlato a Entecavir USP nella soluzione standard (mg/mL)
Cu = concentrazione di Entecavir nella soluzione campione (mg/mL)
Criteri di accettazione: NMT 0,1%
TEST SPECIFICI
• DETERMINAZIONE DELL'ACQUA<921>, Metodo I, Metodo Ic: 5,5%-7,0%
• ROTAZIONE OTTICA<781S>, Procedure, Rotazione specifica
Soluzione campione: 10 mg/mL di Entecavir in una miscela di dimetilformammide e metanolo (50:50)
Criteri di accettazione: da +24° a +30°
REQUISITI AGGIUNTIVI
• IMBALLAGGIO E CONSERVAZIONE: Conservare in contenitori ben chiusi, al riparo dalla luce. Conservare a temperatura ambiente.
• NORME DI RIFERIMENTO USP<11>
USP Entecavir monoidrato RS
Composto A RS correlato a Entecavir USP
3-Benzil-4-silil entecavir;
9-[(1S,3R,4S)-4-Dimetilfenilsilil-3-(benzilossimetile)-2-metilenciclopentil]guanina.
C27H31N5O2Si 485,65
Miscela di idoneità del sistema USP Entecavir RS
La miscela contiene entecavir monoidrato e le seguenti impurezze (possono essere presenti anche altre impurezze):
Entecavir 1-epimero.
8-Entecavir idrossilato.
8-Metossientecavir.