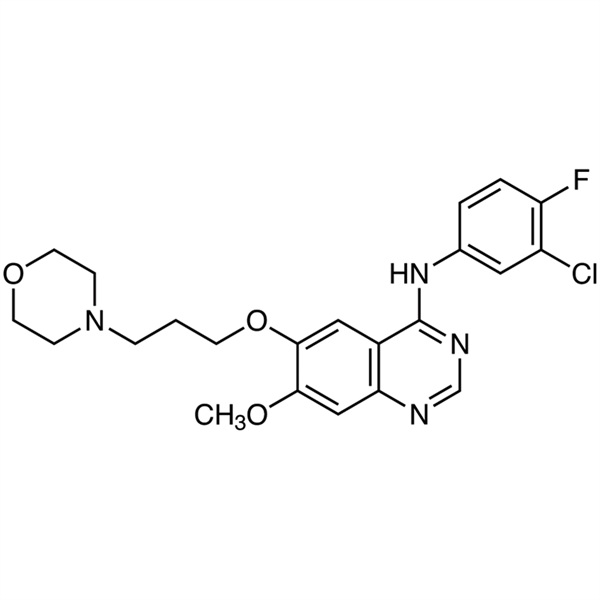
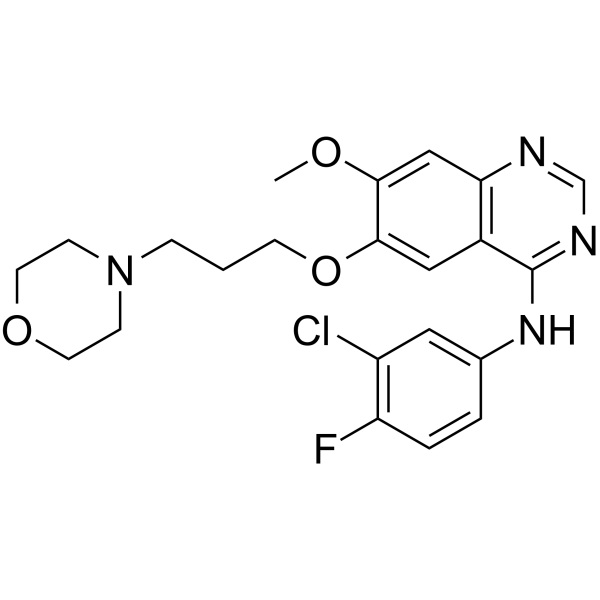
Gefitinib CAS 184475-35-2 Purezza >99,5% (HPLC)
Shanghai Ruifu Chemical Co., Ltd. è il principale produttore di Gefitinib (CAS: 184475-35-2) di alta qualità. Ruifu Chemical è in grado di fornire consegne in tutto il mondo, prezzi competitivi, servizio eccellente e disponibilità di piccole quantità e grandi quantità. Acquistare Gefitinib e intermedi, Si prega di contattare: alvin@ruifuchem.com
| Nome chimico | Gefitinib |
| Sinonimi | Base libera di Gefitinib; Iressa; ZD1839; ZD-1839; N-(3-Cloro-4-fluorofenile)-7-metossi-6-(3-morfolinopropossi)chinazolina-4-ammina; N-(3-Cloro-4-fluorofenile)-7-metossi-6-[3-(4-morfolinil)propossi]-4-chinazolinamina |
| Stato delle scorte | In magazzino, produzione commerciale |
| Numero CAS | 184475-35-2 |
| Formula molecolare | C22H24ClFN4O3 |
| Peso Molecolare | 446,91 g/mol |
| Punto di fusione | Da 194,0 a 198,0 ℃ |
| Densità | 1,322±0,06 g/cm3 |
| Solubilità | Insolubile in acqua. Solubile in DMSO |
| Temp. di conservazione | Temperatura ambiente |
| Spedizione | Ambiente |
| Certificato di autenticità e scheda di sicurezza | Disponibile |
| Origine | Shangai, Cina |
| Categorie di prodotti | API (ingrediente farmaceutico attivo) |
| Marchio | Ruifu chimica |
| Articoli | Standard di ispezione | Risultati |
| Aspetto | Polvere da bianca a spenta-bianca | Conforme |
| Perdita all'essiccazione | <0,50% | 0,13% |
| Residuo sull'accensione | <0,20% | 0,06% |
| Singola impurità | <0,10% | 0,09% |
| Impurità totali | <0,50% | 0,20% |
| Metalli pesanti (Pb) | ≤10 ppm | <10 ppm |
| Purezza di gefitinib | >99,5% (HPLC) | 99,80% |
| Spettro infrarosso | Coerente con la struttura | Conforme |
| Spettro NMR 1H | Coerente con la struttura | Conforme |
| Conclusione | Il prodotto è stato testato ed è conforme alle specifiche fornite | |
Pacchetto: Bottiglia di fluorurato, sacchetto di alluminio, fusto di cartone da 25 kg o in base alle esigenze del cliente.
Condizioni di conservazione: Tenere il contenitore ben chiuso e conservarlo in un magazzino fresco, asciutto e ben ventilato, lontano da sostanze incompatibili. Proteggere dalla luce e dall'umidità.
Spedizione:Consegna in tutto il mondo via aerea, tramite FedEx / DHL Express. Fornire consegne rapide e affidabili.
Non per l'uso negli esseri umani. Non per uso diagnostico o terapeutico. Solo per uso nella ricerca in vitro.
Nessun prodotto verrà fornito in Paesi nei quali ciò potrebbe essere in conflitto con i brevetti esistenti. Tuttavia la responsabilità finale spetta all'Acquirente.
Come acquistare? Si prega di contattareDr. Alvin Huang: sales@ruifuchem.com o alvin@ruifuchem.com
15 anni di esperienza?Abbiamo più di 15 anni di esperienza nella produzione ed esportazione di un'ampia gamma di prodotti farmaceutici intermedi o di prodotti di chimica fine di alta qualità.
Mercati principali? Vendi al mercato interno, Nord America, Europa, India, Corea, Giappone, Australia, ecc.
Vantaggi? Qualità superiore, prezzo conveniente, servizi professionali e supporto tecnico, consegna rapida.
Qualità Assicurazione? Sistema di controllo qualità rigoroso. Le apparecchiature professionali per l'analisi includono NMR, LC-MS, GC, HPLC, ICP-MS, UV, IR, OR, K.F, ROI, LOD, MP, chiarezza, solubilità, test del limite microbico, ecc.
Campioni? La maggior parte dei prodotti fornisce campioni gratuiti per la valutazione della qualità, i costi di spedizione sono a carico dei clienti.
Audit di fabbrica? Benvenuto dell'audit di fabbrica. Si prega di fissare un appuntamento in anticipo.
MOQ? Nessun MOQ. Il piccolo ordine è accettabile.
Tempi di consegna? Se disponibile in magazzino, consegna garantita in tre giorni.
Trasporti? Per espresso (FedEx, DHL), per via aerea, via mare.
Documenti? Servizio post-vendita: possono essere forniti COA, MOA, ROS, MSDS, ecc.
Sintesi personalizzata? Può fornire servizi di sintesi personalizzati per soddisfare al meglio le vostre esigenze di ricerca.
Termini di pagamento? La fattura proforma verrà inviata prima dopo la conferma dell'ordine, allegata alle nostre coordinate bancarie. Pagamento tramite T/T (trasferimento telex), PayPal, Western Union, ecc.
| Descrizione di sicurezza | 24/25- Evitare il contatto con la pelle e gli occhi. |
| Codice SA | 2934999099 |
Gefitinib (CAS: 184475-35-2) è un farmaco terapeutico mirato anti-tumorale altamente specifico sviluppato da AstraZeneca, Regno Unito. È il primo farmaco a bersaglio molecolare per il trattamento del cancro polmonare non a piccole cellule. Agisce inibendo selettivamente la via di trasduzione del segnale del recettore tirosina chinasi del fattore di crescita epidermico (EGFR-TK). Il fattore di crescita epidermico (EGF) è un polipeptide con una massa molecolare relativa di 6,45 × 103, che può combinarsi con il recettore del fattore di crescita epidermico (EGFR) sulla membrana cellulare bersaglio per produrre effetti biologici. L'EGFR è un recettore di tipo tirosina chinasi (TK). Quando si lega all'EGF, può promuovere l'attivazione della TK nel corpo ricevente, con conseguente autofosforilazione dei residui di tirosina del recettore, fornendo segnali di divisione continua alle cellule, causando proliferazione e differenziazione cellulare. L’EGFR è abbondante nei tessuti umani ed è altamente espresso nei tumori maligni. Bloccando la via di segnalazione dell’EGFR sulla superficie cellulare, gefitinib ostacola la crescita del tumore, le metastasi e l’angiogenesi e può indurre l’apoptosi delle cellule tumorali. Nell'agosto 2002, gefitinib è stato commercializzato per la prima volta in Giappone come trattamento di prima linea per il cancro del polmone non a piccole cellule con il nome commerciale Iressa. Nel maggio 2003, la Food and Drug Administration statunitense ha approvato gefitinib come monoterapia di terza linea per i pazienti con carcinoma polmonare non a piccole cellule avanzato che erano inefficaci con i farmaci antitumorali a base di platino e la chemioterapia con docetaxel. Attualmente è stato approvato da Australia, Giappone, Argentina, Singapore e Corea del Sud per il trattamento del cancro polmonare non a piccole cellule in stadio avanzato. Il 28 febbraio 2005, la China Food and Drug Administration ha approvato gefitinib per il trattamento del cancro polmonare non a piccole cellule (NSCLC) localmente avanzato o metastatico precedentemente sottoposto a chemioterapia. Attualmente non è approvato per l'uso come terapia di prima linea per il NSCLC avanzato. Il 1° luglio 2009, l'Agenzia Europea per i Medicinali ha approvato ufficialmente gefitinib per il trattamento di prima linea, seconda e terza linea del carcinoma polmonare non a piccole cellule localmente avanzato o metastatico con mutazioni del gene EGFR negli adulti.