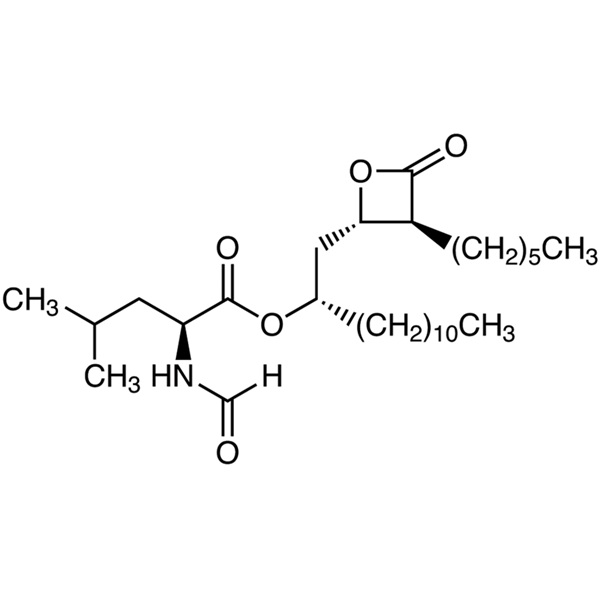
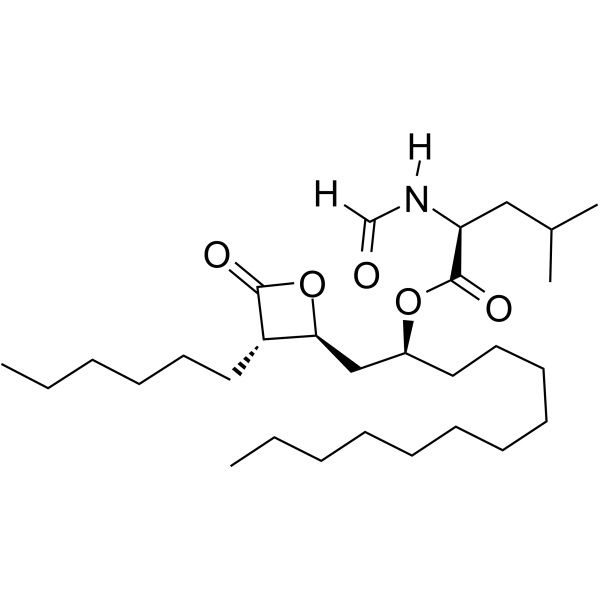
Purezza 98,0~101,5% del farmaco dimagrante Orlistat CAS 96829-58-2 API
Shanghai Ruifu Chemical Co., Ltd. è il principale produttore di Orlistat (CAS: 96829-58-2) con una produzione commerciale di farmaci dimagranti di alta qualità. Ruifu Chemical è in grado di fornire consegne in tutto il mondo, prezzi competitivi, servizio eccellente e disponibilità di piccole quantità e grandi quantità. Acquista Orlistat, Si prega di contattare: alvin@ruifuchem.com
| Nome chimico | Orlistat |
| Sinonimi | N-Formile-L-Leucina (1S)-1-[[(2S,3S)-3-Esil-4-Oxo-2-Ossetanil]Metile] Dodecile estere; (S)-2-Formilammino-4-Metil-Acido pentanoico (S)-1-[[(2S,3S)-3-Esil-4-Oxo-2-Ossetanil]Metil]-Dodecile estere ; Tetraidrolipstatina; Ro-18-0647 |
| Numero CAS | 96829-58-2 |
| Stato delle scorte | Disponibile, la produzione arriva fino a tonnellate |
| Formula molecolare | C29H53NO5 |
| Peso Molecolare | 495,75 |
| Punto di fusione | 43,0 ℃ ~ 48,0 ℃ |
| Densità | 0,976±0,06 g/cm3 |
| Sensibile | Sensibile al calore |
| Solubilità | Solubile in cloroformio |
| Condizioni di spedizione | A temperatura ambiente |
| Certificato di autenticità e scheda di sicurezza | Disponibile |
| Marchio | Ruifu chimica |
| Articolo | Specifiche |
| Aspetto | Polvere cristallina bianca o quasi bianca |
| Identificazione A | Assorbimento degli infrarossi |
| Identificazione B | Il tempo di ritenzione del picco maggiore della soluzione Campione corrisponde a quello della soluzione Standard, come ottenuto nel dosaggio. |
| Metodo di purezza/analisi | 98,0~101,5% di C29H53NO5, calcolato su base anidra, priva di solventi- |
| Rotazione specifica | -48,0° ~ -51,0° |
| Determinazione dell'acqua | ≤0,20% |
| Residuo all'accensione | ≤0,10% |
| Metalli pesanti | ≤20 ppm |
| Composto correlato a Orlistat A | ≤0,20% |
| Composto correlato a Orlistat B | ≤0,05% |
| Formilleucinea | ≤0,20% |
| Composto correlato a Orlistat C | ≤0,05% |
| Epimero ad anello aperto Orlistat | ≤0,20% |
| D-Leucina Orlistat | ≤0,20% |
| Impurità individuale non identificata | ≤0,10% |
| Composto correlato a Orlistat D | ≤0,20% |
| Ammide ad anello aperto di Orlistat | ≤0,10% |
| Composto correlato a Orlistat E | ≤0,20% |
| Impurità totali | ≤1,00% |
| Prova standard | Farmacopea cinese; USP35 |
| Utilizzo | Ingrediente farmaceutico attivo (API) |
Pacchetto: Bottiglia, sacchetto di alluminio, tamburo di cartone da 25 kg o secondo le esigenze del cliente.
Condizioni di conservazione: Tenere il contenitore ben chiuso e conservarlo in un magazzino fresco, asciutto (2~8℃) e ben ventilato, lontano da sostanze incompatibili. Stare lontano dalla luce forte, dal calore e dall'umidità.
Spedizione: Consegna in tutto il mondo via aerea, tramite FedEx / DHL Express. Fornire consegne rapide e affidabili.

Orlistat è una nuova forma di farmaco dimagrante riconosciuta a livello internazionale. Il suo nome commerciale è Sainike ed è stato messo in vendita per la prima volta in Nuova Zelanda nel 1998. Orlistat è un inibitore specifico della lipasi gastrointestinale a lungo termine e altamente efficace ed è insolubile in acqua, solubile in cloroformio e facilmente solubile in etanolo. Orlistat può essere utilizzato clinicamente per trattare l’obesità. Di solito, una dose di 120 mg viene assunta tre volte al giorno entro un'ora dal pasto. La perdita di peso inizia a verificarsi dopo due settimane di utilizzo. Può essere utilizzato continuamente per 6-12 mesi e i suoi effetti cesseranno di aumentare quando la dose giornaliera supera i 400 mg. Questo farmaco è adatto per essere utilizzato in combinazione con una dieta ipocalorica da parte di individui obesi e in sovrappeso e può anche essere utilizzato come trattamento a lungo termine per pazienti che hanno affrontato fattori di rischio correlati al peso. Orlistat ha un effetto di controllo del peso a lungo termine che riduce e mantiene il peso e previene i rimbalzi. L'uso di Orlistat può ridurre l'insorgenza di fattori di rischio e malattie legati al peso, tra cui ipercolesterolemia, diabete di tipo 2, ridotta tolleranza al glucosio, iperinsulinemia e ipertensione, e può ridurre il contenuto di grassi negli organi. Orlistat regola anche i livelli di lipidi nel sangue: può diminuire i trigliceridi sierici (TG) e il colesterolo lipoproteico a bassa densità (LDL-C) e può aumentare il rapporto tra lipoproteine ad alta densità e lipoproteine a bassa densità nei pazienti obesi.
Orlistat
C29H53NO5 495.73
l-Leucina, N-formil-, 1-[(3-esil-4-osso-2-ossetanil)metil]dodecil estere, [2S-[2(R*), 3]]-;
N-Formil-l-leucina, estere con (3S,4S)-3-esil-4-[(2S)-2-idrossitridecil]-2-oxetanone [96829-58-2].
DEFINIZIONE
Orlistat contiene NLT 98,0% e NMT 101,5% di C29H53NO5, calcolato su base anidra, priva di solventi-.
IDENTIFICAZIONE
• A. Assorbimento degli infrarossi<197M>
• B. Il tempo di ritenzione del picco maggiore della soluzione campione corrisponde a quello della soluzione standard, come ottenuto nel test.
SAGGIO
• Procedura
[Nota-Evitare l'uso di matracci di plastica per la preparazione o il contenimento di qualsiasi soluzione in questa analisi. ]
Fase mobile: acetonitrile, acido fosforico e acqua (860: 0,05: 140)
Soluzione standard: 0,5 mg/mL di USP Orlistat RS in fase mobile. Iniettare immediatamente dopo la preparazione o conservare alle 5.
Soluzione campione: 0,5 mg/mL di Orlistat in fase mobile. Iniettare immediatamente dopo la preparazione o conservare alle 5.
Sistema cromatografico
(Vedere Cromatografia<621>, Idoneità del sistema.)
Modalità:LC
Rivelatore: UV 195
Colonna: 3,9-mm × 15-cm; 4-μm imballaggio L1
Velocità di flusso: 1,0 ml/min
Dimensione dell'iniezione: 20 µl
Idoneità del sistema
Campione: soluzione standard
Requisiti di idoneità
Deviazione standard relativa: NMT 2,0%
Analisi
Campioni: soluzione standard e soluzione campione
Calcolare la percentuale di orlistat (C29H53NO5) nella porzione di Orlistat assunta:
Risultato = (rU/rS) × (CS/CU) × 100
rU = risposta di picco dalla soluzione campione
rS = risposta di picco dalla soluzione standard
CS = concentrazione di USP Orlistat RS nella soluzione standard (mg/mL)
CU = concentrazione di Orlistat nella soluzione campione (mg/mL)
Criteri di accettazione: 98,0%-101,5% su base anidra, priva di solventi-
IMPURITÀ
Impurezze inorganiche
• Residuo all'accensione<281>: NMT 0,1%
• Metalli pesanti, Metodo II<231>: 20 ppm
Impurità organiche
• Procedura 1: Limite del composto A correlato a Orlistat
Soluzione standard: 0,1 mg/mL di composto A RS correlato a Orlistat USP in acetone
Soluzione campione: 50 mg/mL di Orlistat in acetone
Sistema cromatografico
(Vedere Cromatografia<621>, Cromatografia su strato sottile.)
Modalità: TLC
Adsorbente: strato di 0,25-mm di miscela cromatografica di gel di silice
Volume di applicazione: 10 µl
Sistema solvente di sviluppo: toluene e acetato di etile (4:1)
Soluzione di rilevazione: trasferire 2,5 g di acido fosfomolibdico e 1 g di solfato cerrico in un matraccio tarato da 100-mL, sciogliervi e diluire con metanolo fino al volume.
Analisi
Campioni: soluzione standard e soluzione campione
Rimuovere la piastra e asciugarla accuratamente all'aria. Spruzzare la piastra essiccata con la soluzione di rilevamento e posizionare la piastra in un forno a 120 per 30 minuti.
Criteri di accettazione: qualsiasi macchia secondaria della soluzione campione corrispondente al composto A correlato a orlistat non è più intensa della macchia corrispondente della soluzione standard (0,2%).
• Procedura 2: Limite del composto B correlato a Orlistat
Soluzione standard: 0,025 mg/ml di composto B RS correlato a Orlistat USP in cloruro di metilene
Soluzione campione: 50 mg/mL di Orlistat in cloruro di metilene
Soluzione campione arricchita: 50 mg/mL di Orlistat in soluzione standard
Sistema cromatografico
(Vedere Cromatografia<621>, Idoneità del sistema.)
Modalità: GC
Rivelatore: Ionizzazione di fiamma
Colonna: silice fusa da 0,32-mm x 30-m, rivestita con una fase stazionaria G27 da 0,25-μm
Temperatura della colonna: vedere la tabella dei programmi di temperatura di seguito.
Temperatura iniziale () Rampa di temperatura (/min) Temperatura finale () Tempo di mantenimento alla temperatura finale (min)
50 4 170 -
170 30 300 30
Temperatura
Iniettore: 270
Rivelatore: 280
Gas di trasporto: elio
Portata: 30 ml/min
Rapporto di divisione: 10:1
Dimensione dell'iniezione: 2 µl
Idoneità del sistema
Campione: soluzione standard
Requisiti di idoneità
Deviazione standard relativa: NMT 10,0%
Analisi
Campioni: soluzione campione e soluzione campione arricchita
Calcolare la percentuale del composto B correlato a orlistat nella porzione di Orlistat presa:
Risultato = [rU/(rSP rU)] × (CS/CT) × 100
rU = risposta di picco del composto B correlato a orlistat dalla soluzione campione
rSP = risposta di picco del composto B correlato a orlistat dalla soluzione campione arricchita
CS = concentrazione del composto B RS correlato a USP Orlistat nella soluzione standard (mg/mL)
CT = concentrazione di Orlistat nella soluzione campione arricchita (mg/mL)
Criteri di accettazione: è stato trovato NMT 0,05% del composto B correlato a orlistat.
• Procedura 3
[Nota-Evitare l'uso di matracci di plastica per la preparazione o il contenimento di qualsiasi soluzione in questa analisi. ]
Fase mobile, soluzione standard e soluzione campione: preparare come indicato nel dosaggio.
Soluzione di idoneità del sistema: 10 µg/ml di USP Orlistat RS, 0,1 µg/ml di USP Orlistat Related Compound C RS e 0,25 µg/ml di USP Orlistat Related Compound D RS in fase mobile
Sistema cromatografico
(Vedere Cromatografia<621>, Idoneità del sistema.)
Procedere come indicato nel dosaggio, tranne che per cromatografare la soluzione di idoneità del sistema.
Idoneità del sistema
Esempio: soluzione di idoneità del sistema
Requisiti di idoneità
Rapporto segnale-/rumore: NLT 3 per i picchi del composto C correlato a orlistat e del composto D correlato a orlistat
Deviazione standard relativa: NMT 10,0% per il picco dell'orlistat
Analisi
Campioni: soluzione standard e soluzione campione
Calcolare la percentuale di ciascuna impurità nella porzione di Orlistat prelevata:
Risultato = (rU/rS) × (CS/CU) × (1/F) × 100
rU = risposta di picco per ogni singola impurità dalla soluzione campione
rS = risposta di picco dell'USP Orlistat RS dalla soluzione standard
CS = concentrazione di USP Orlistat RS nella soluzione standard (mg/mL)
CU = concentrazione di Orlistat nella soluzione campione (mg/mL)
F = fattore di risposta relativo come indicato nella Tabella delle impurità 1
Criteri di accettazione: vedere la tabella delle impurità 1.
Impurezza Tabella 1
Nome Tempo di ritenzione relativo Fattore di risposta relativo Criteri di accettazione, NMT (%)
Formilleucinea 0,10 4,0 0,2
Composto correlato all'orlistat C 0,13 33 0,05
Orlistat epimerbo ad anello aperto 0,44 1,0 0,2
Composto correlato a Orlistat D* 0,90 - Calcolato nel
Procedura 4
Orlistat anello aperto amidec* 0,90 - Calcolato nel
Procedura 4
Orlistat 1.00 - -
d-Leucina orlistatd 1,18 1,0 0,2
Impurità individuale non identificata - 1,0 0,1
* Coeluti in questo sistema LC, determinati utilizzando la Procedura 4.
a N-Formil-l-leucina.
b (2S,3R,5S)-5-[(S)-2-formilammino-4-metil-pentanoilossi]-2-esil-3-idrossi-acido esadecanoico.
c N-Formil-l-leucina (S)-1-[(2S,3S)-2-idrossi-3-[1-fenil-R-etilcarbomoil]nonil]-dodecil estere.
d N-Formil-d-leucina (S)-1-[[(2S,3S)-3-esil-4-osso-2-ossetanil]metil]dodecil estere o enantiomero.
• Procedura 4: Limite del composto correlato a Orlistat D
Fase mobile: metanolo e acqua (83:17)
Soluzione di idoneità del sistema: 4 mg/ml di USP Orlistat RS e 2,4 µg/ml di USP Orlistat Related Compound D RS in acetonitrile, rispettivamente
Soluzione standard: 5,0 mg/mL di USP Orlistat RS in acetonitrile
Soluzione campione: 5,0 mg/mL di Orlistat in acetonitrile
Sistema cromatografico
(Vedere Cromatografia 621, Idoneità del sistema.)
Modalità:LC
Rivelatore: 205 nm
Colonna: 4,0-mm × 25-cm; 5-μm baderna L7
Portata: 0,6 ml/min
Dimensione dell'iniezione: 20 µl
Idoneità del sistema
Esempio: soluzione di idoneità del sistema
Requisiti di idoneità
Rapporto segnale-rumore: NLT 3 per il picco D del composto correlato a orlistat
Deviazione standard relativa: NMT 10,0% per il picco dell'orlistat
Analisi
Campioni: soluzione standard e soluzione campione
Calcolare la percentuale di ciascuna impurità nella porzione di Orlistat prelevata:
Risultato = (rU/rS) × (CS/CU) × (1/F) × 100
rU = risposta di picco per ogni singola impurità dalla soluzione campione
rS = risposta di picco per USP Orlistat RS dalla soluzione standard
CS = concentrazione di USP Orlistat RS nella soluzione standard (μg/mL)
CU = concentrazione di Orlistat nella soluzione campione (μg/mL)
F = fattore di risposta relativo ottenuto nella Tabella 2 delle impurità
Criteri di accettazione: vedere la tabella delle impurezze 2.
Impurezza Tabella 2
Nome Tempo di ritenzione relativo Fattore di risposta relativo Criteri di accettazione, NMT (%)
Composto correlato all'orlistat D 0,94 1,0 0,2
Orlistat 1.00 - -
Orlistat ad anello aperto amidea 1,25 4,3 0,1
un N-formil-l-leucina (S)-1-[(2S,3S)-2-idrossi-3-[1-fenil-R-etilcarbomoil]nonil]-dodecil estere.
• Procedura 5: Limite del composto correlato a Orlistat E
Tampone: soluzione di borato 0,4 N, regolata a un pH di 10,2
Agente derivatizzante: soluzione di o-ftaldeide (OPA). [Nota-Se non è possibile ottenerlo in commercio, l'agente derivatizzante può essere preparato come 1% ciascuno di acido 3-mercaptopropionico e o-ftaldialdeide in una soluzione tampone borato 0,4 M.]
Soluzione A: trasferire 4,1 g di sodio acetato triidrato e 40 mg di acido etilendiamminotetraacetico (EDTA) in un matraccio tarato da 1-L. Sciogliere in 950 mL di acqua e regolare con idrossido di sodio 0,1 N fino a un pH di 7,2. Diluire con acqua a volume, aggiungere 2,5 mL di tetraidrofurano e mescolare. Filtrare e degassare.
Soluzione B: trasferire 2,7 g di sodio acetato triidrato e 40 mg di EDTA in un matraccio tarato da 1-L. Sciogliere in 200 mL di acqua e regolare con idrossido di sodio 0,1 N fino a un pH di 7,2. Aggiungere 800 ml di acetonitrile, filtrare e degassare.
Fase mobile: vedere la tabella dei gradienti di seguito.
Tempo (min) Soluzione A (%) Soluzione B (%)
0 96,7 3.3
20 60 40
24 0 100
38 0 100
38 96,7 3.3
45 96,7 3.3
Soluzione standard: trasferire una quantità pesata di circa 0,2 mg del composto E RS correlato all'Orlistat USP in una fiala da 20-mL di spazio di testa-. Aggiungere 10 ml di idrossido di sodio 4 N e chiudere la fiala. Riscaldare la fiala a 100 per 1 ora, quindi lasciarla raffreddare a temperatura ambiente. Trasferire 2 mL della soluzione risultante in un matraccio tarato da 50-mL e diluire con acqua a volume. A 0,5 ml di questa soluzione aggiungere 2,0 ml di tampone e 0,5 ml di agente derivatizzante.
Soluzione campione: procedere come indicato per la soluzione standard, ma utilizzare invece 25 mg di Orlistat per sostituire 0,2 mg di USP Orlistat Related Compound E RS.
Sistema cromatografico
(Vedere Cromatografia<621>, Idoneità del sistema.)
Modalità:LC
Rivelatore: Fluorescenza 340 nm (eccitazione); 450 nm (emissione)
Colonne
Protezione: 2,1-mm × 2-cm; Confezione da 50-μm L1
Analitico: 2,1-mm × 20-cm; imballaggio L1
Portata: 0,5 ml/min
Dimensione dell'iniezione: 20 µl
Idoneità del sistema
Campione: soluzione standard
Requisiti di idoneità
Deviazione standard relativa: NMT 6,0% per il picco del composto E correlato a orlistat
Analisi
Campioni: soluzione standard e soluzione campione
Calcolare la percentuale di questa impurità nella porzione di Orlistat prelevata:
Risultato = (rU/rS) × (CS/CU) × 100
rU = risposta di picco per il composto E correlato a orlistat nella soluzione campione
rS = risposta di picco per il composto E RS correlato a Orlistat USP nella soluzione standard
CS = concentrazione del composto E RS correlato a USP Orlistat nella soluzione standard (mg/mL)
CU = concentrazione di Orlistat nella soluzione campione (mg/mL)
Criteri di accettazione
Impurezza individuale: si trova NMT 0,2% del composto E correlato a orlistat.
Impurezze totali: viene trovato NMT 1,0% delle impurità totali, vengono aggiunti i risultati delle Procedure 1, 2, 3, 4 e 5.
TEST SPECIFICI
• Rotazione ottica, Rotazione specifica<781>
Soluzione del campione: 30 mg/mL in alcool disidratato
Criteri di accettazione: Tra -48.0 e -51.0, a 20
• Determinazione dell'acqua, metodo Ic<921>: NMT 0,2%
REQUISITI AGGIUNTIVI
• Imballaggio e conservazione: conservare in contenitori ben chiusi a una temperatura compresa tra 2 e 8 ℃.
• Standard di riferimento USP<11>
USP Orlistat RS
Composto A RS correlato a USP Orlistat
Composto B RS correlato a USP Orlistat
Composto C RS correlato a USP Orlistat
Composto D RS correlato a USP Orlistat
Composto correlato a USP Orlistat E RS
USP35