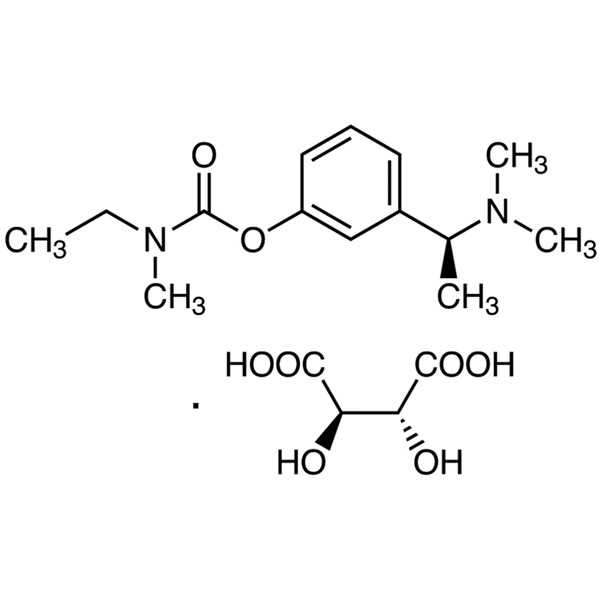
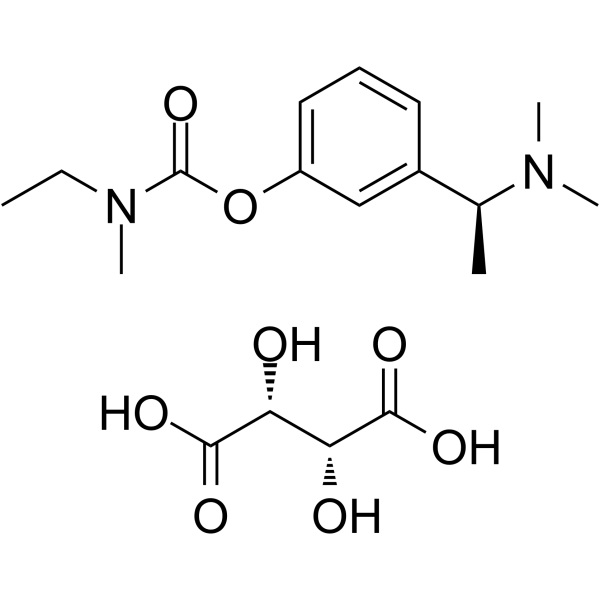
Test di rivastigmina tartrato CAS 129101-54-8 98,0~102,0
Shanghai Ruifu Chemical Co., Ltd. è il principale produttore di tartrato di rivastigmina (CAS: 129101-54-8) di alta qualità. Ruifu Chemical è in grado di fornire consegne in tutto il mondo, prezzi competitivi, servizio eccellente e disponibilità di piccole quantità e grandi quantità. Acquistare rivastigmina tartrato, Si prega di contattare: alvin@ruifuchem.com
| Nome chimico | Rivastigmina tartrato |
| Sinonimi | Exelon; ENA-713; Rivastigmina L-Tartrato; Rivastigmina idrogeno tartrato; CS-118; S-Rivastigmina tartrato; 3-[(S)-1-(Dimetilammino)etil]fenil N-Etil-N-Metilcarbammato L-Tartrato; N-Etil-N-Metilcarbammico Acido 3-[(S)-1-(Dimetilammino)etil]fenil Estere L-Tartrato |
| Stato delle scorte | In magazzino, produzione commerciale |
| Numero CAS | 129101-54-8 |
| CAS correlato | 123441-03-2 |
| Formula molecolare | C14H22N2O2·C4H6O6 |
| Peso Molecolare | 400,43 g/mol |
| Punto di fusione | Da 124,0 a 128,0 ℃ |
| Rotazione specifica [a]20/D | Da +4,0° a +7,0° (C=5, metanolo) |
| Solubilità | Solubile in metanolo |
| Certificato di autenticità e scheda di sicurezza | Disponibile |
| Origine | Shangai, Cina |
| Marchio | Ruifu chimica |
| Articoli | Standard di ispezione | Risultati |
| Aspetto | Polvere cristallina da bianca a spenta-bianca | Conforme |
| Analisi | 98,0~102,0% (su base anidra) | 99,8% |
| Acqua di Karl Fischer | ≤0,50% | 0,15% |
| Residuo sull'accensione | ≤0,10% | 0,07% |
| Metalli pesanti (Pb) | ≤20 ppm | <10 ppm |
| Impurità fenolica | ≤0,30% | <0,30% |
| DPTTA | ≤0,15% | <0,15% |
| Né impurità | ≤0,15% | <0,15% |
| Impurità di carbammato | ≤0,15% | <0,15% |
| Impurità dell'etere | ≤0,15% | <0,15% |
| Qualsiasi altra impurità | ≤0,10% | <0,10% |
| Impurità totali | ≤0,50% | <0,50% |
| R-Enantiomero | ≤0,30% | <0,30% |
| Spettro infrarosso | Coerente con la struttura | Conforme |
| Spettro NMR 1H | Coerente con la struttura | Conforme |
| Conclusione | Il prodotto è stato testato ed è conforme allo standard USP35 | |
Pacchetto: Bottiglia di fluorurato, sacchetto di alluminio, fusto di cartone da 25 kg o in base alle esigenze del cliente.
Condizioni di conservazione: Tenere il contenitore ben chiuso e conservarlo in un magazzino fresco, asciutto (2~8℃) e ben ventilato, lontano da sostanze incompatibili. Proteggere dalla luce e dall'umidità.
Spedizione:Consegna in tutto il mondo via aerea, tramite FedEx / DHL Express. Fornire consegne rapide e affidabili.
Rivastigmina tartrato
C14H22N2O2·C4H6O6 400,42
Acido etilmetilcarbammico, 3-[(S)-1-(dimetilammino)etil]fenil estere, (2R,3R)-2,3-diidrossibutandioato;
(S)-3-[1-(Dimetilammino)etil]fenil etilmetilcarbammato, tartrato di idrogeno [129101-54-8].
Rivastigmina 250,34 [123441-03-2].
DEFINIZIONE
Rivastigmina tartrato contiene NLT 98,0% e NMT 102,0% della quantità indicata in etichetta di C14H22N2O2·C4H6O6, calcolata su base anidra.
IDENTIFICAZIONE
• A. Assorbimento degli infrarossi<197K>
• B. Il tempo di ritenzione del picco maggiore della soluzione del campione corrisponde a quello della soluzione di idoneità del sistema, come ottenuto nel test per le impurità organiche, Procedura 2: Purezza enantiomerica.
SAGGIO
• Procedura
Tampone: 8,6 mg/mL di fosfato di ammonio monobasico. Regolare con una soluzione di ammoniaca ad un pH di 7,0.
Fase mobile: metanolo, acetonitrile e tampone (15:15:70)
Soluzione adatta al sistema: 0,05 mg/ml ciascuno di composto A RS correlato alla rivastigmina USP e composto B RS correlato alla rivastigmina USP in fase mobile
Soluzione standard: 0,2 mg/mL di USP Rivastigmine Tartrate RS in fase mobile
Soluzione campione: 0,2 mg/mL di Rivastigmina Tartrato in fase Mobile
Sistema cromatografico
(Vedere Cromatografia<621>, Idoneità del sistema.)
Modalità:LC
Rivelatore: UV 215 nm
Colonna: 4,6-mm × 25-cm; 5-μm baderna L7
Portata: 1,2 ml/min
Dimensione dell'iniezione: 20 µl
[Nota-La velocità del flusso può essere regolata a 1,5 ml/min, se necessario, per ottenere un tempo di ritenzione raccomandato della rivastigmina pari a circa 10 minuti. ]
Idoneità del sistema
Esempi: soluzione di idoneità del sistema e soluzione standard
Requisiti di idoneità
Risoluzione: NLT 1,5 tra il composto A correlato alla rivastigmina e il composto B correlato alla rivastigmina, soluzione di idoneità del sistema
Efficienza della colonna: piastre teoriche NLT 5000, soluzione Standard
Fattore di scodamento: NMT 3.0, soluzione standard
Deviazione standard relativa: NMT 2,0%, Soluzione standard
Analisi
Campioni: soluzione standard e soluzione campione
Calcolare la percentuale di C14H22N2O2·C4H6O6 nella porzione di Rivastigmina Tartrato assunta:
Risultato = (rU/rS) × (CS/CU) × 100
rU = risposta di picco dalla soluzione campione
rS = risposta di picco dalla soluzione standard
CS = concentrazione della soluzione standard (mg/mL)
CU = concentrazione della soluzione campione (mg/mL)
Criteri di accettazione: 98,0%-102,0% su base anidra
IMPURITÀ
Impurezze inorganiche
• Residuo all'accensione<281>: NMT 0,1%
• Metalli pesanti, Metodo II<231>: NMT 20 ppm
Impurità organiche
• Procedura 1
Soluzione per la fase mobile e l'idoneità del sistema: procedere come indicato nel dosaggio.
Soluzione standard: 1,0 µg/mL di USP Rivastigmine Tartrate RS in fase mobile
Soluzione campione: 1,0 mg/ml di rivastigmina tartrato in fase mobile
Sistema cromatografico: procedere come indicato nel dosaggio.
(Vedere Cromatografia<621>, Idoneità del sistema.)
Idoneità del sistema
Esempi: soluzione di idoneità del sistema e soluzione standard
Requisiti di idoneità
Risoluzione: NLT 1,5 tra il composto A correlato alla rivastigmina e il composto B correlato alla rivastigmina, soluzione di idoneità del sistema
Deviazione standard relativa: NMT 10%, Soluzione standard
Analisi [Nota-Il tempo di analisi è 8 volte il tempo di ritenzione del picco della rivastigmina. ]
Campioni: soluzione standard e soluzione campione
Calcolare la percentuale di ogni singola impurità presente nella porzione di Rivastigmina Tartrato assunta:
Risultato = (rU/rS) × (CS/CU) × (1/F) × 100
rU = risposta di picco per ciascuna impurità dalla soluzione campione
rS = risposta di picco dalla soluzione standard
CS = concentrazione di USP Rivastigmine Tartrate RS nella soluzione standard (mg/mL)
CU = concentrazione di rivastigmina tartrato nella soluzione campione (mg/mL)
F = fattore di risposta relativo (vedere Tabella delle impurità 1)
Criteri di accettazione
Impurezze individuali: vedere la tabella delle impurezze 1.
Impurezze totali: NMT 0,5%
Impurezza Tabella 1
| Nome | Tempo di conservazione relativo | Fattore di risposta relativo | Criteri di accettazione NMT% |
| Tartrato | 0,18 | — | Ignorare |
| Impurità fenoliche | 0,28 | 1.6 | 0,3 |
| DPTTAb | 0,46 | 0,83 | 0,15 |
| Né impuro | 0,57 | 1.2 | 0,15 |
| Rivastigmina | 1.0 | 1.0 | — |
| Carbammato impuro | 4.1 | 1.3 | 0,15 |
| Impurità dell'etere | 6.5 | 1.4 | 0,15 |
| Qualsiasi altra impurità | — | 1.0 | 0,1 |
un (S)-3-[1-(Dimetilammino)etil]fenolo.
b (+)-Di-(p-toluoil)-d-acido tartarico (composto A correlato alla rivastigmina).
c (S)-3-[1-(Dimetilammino)etil]fenil dimetilcarbammato (composto B correlato alla rivastigmina).
d 3-Nitrofenil etil(metil)carbammato.
e (S)-N,N-Dimetil-1-[3-(4-nitrofenossi)fenil]etanamina.
• Procedura 2: Purezza enantiomerica
Tampone: trasferire 1,78 g di sodio fosfato bibasico diidrato e 1,38 g di sodio fosfato monobasico in un matraccio tarato da 1000-mL. Sciogliere e diluire con acqua a volume. Regolare con acido fosforico ad un pH di 6,0.
Fase mobile: trasferire 20 mL di acetonitrile e 205 µL di N,N-dimetilottilammina in un matraccio tarato da 1000-mL e diluire con il tampone a volume.
Soluzione standard: 0,1 µg/mL di USP Rivastigmine Tartrate R-Isomer RS in fase mobile
Soluzione di sensibilità: 0,05 µg/mL di USP Rivastigmine Tartrate R-Isomer RS in fase mobile, soluzione standard
Soluzione di idoneità del sistema: 100 µg/mL di USP Rivastigmine Tartrate RS e 0,1 µg/mL di USP Rivastigmine Tartrate R-Isomer RS in fase mobile
Soluzione campione: 100 µg/mL di Rivastigmina Tartrato in fase Mobile
Sistema cromatografico
(Vedere Cromatografia<621>, Idoneità del sistema.)
Modalità:LC
Rivelatore: UV 200 nm
Colonna: 4,0-mm × 10-cm; imballaggio L41
Portata: 0,5 ml/min
Dimensione dell'iniezione: 20 µl
Idoneità del sistema
Campioni: soluzione standard, soluzione di sensibilità e soluzione di idoneità del sistema
Requisiti di idoneità
Risoluzione: NLT 0,8 tra i picchi dell'enantiomero, soluzione di idoneità del sistema
[Nota-L'ordine di eluizione è R-enantiomero, seguito dal picco della rivastigmina, che è S-enantiomero. ]
Rapporto segnale-rumore: NLT 10, soluzione di sensibilità
Deviazione standard relativa: NMT 10%, Soluzione standard
Analisi
Campioni: soluzione standard e soluzione campione
Calcolare la percentuale di R-enantiomero nella porzione di Rivastigmina Tartrato assunta:
Risultato = (rU/rS) × (CS/CU) × 100
rU = risposta di picco dell'enantiomero R-dalla soluzione campione
rS = risposta di picco dell'enantiomero R-dalla soluzione standard
CS = concentrazione di R-enantiomero nella soluzione Standard (μg/mL)
CU = concentrazione di rivastigmina tartrato nella soluzione campione (μg/mL)
Criteri di accettazione: NMT 0,3% dell'enantiomero R-
TEST SPECIFICI
• Determinazione dell'acqua, metodo Ia<921>: NMT 0,5%
REQUISITI AGGIUNTIVI
• Imballaggio e conservazione: conservare in contenitori stretti e conservare a temperatura ambiente.
• Standard di riferimento USP<11>
USP Rivastigmina Tartrato RS
Composto A RS correlato alla rivastigmina USP
Di-p-toluoyl-d-(+)-acido tartarico monoidrato.
C20H20O9 404.37
Composto B RS correlato alla rivastigmina USP
Estere N,N-acido dimetilcarbammico-3-[1-(dimetilammino)etil]fenil.
C13H20N2O2 236,32
USP Rivastigmina Tartrato R-Isomero RS
Come acquistare? Si prega di contattareDr. Alvin Huang: sales@ruifuchem.com o alvin@ruifuchem.com
15 anni di esperienza?Abbiamo più di 15 anni di esperienza nella produzione ed esportazione di un'ampia gamma di prodotti farmaceutici intermedi o di prodotti di chimica fine di alta qualità.
Mercati principali? Vendi al mercato interno, Nord America, Europa, India, Corea, Giappone, Australia, ecc.
Vantaggi? Qualità superiore, prezzo conveniente, servizi professionali e supporto tecnico, consegna rapida.
Qualità Assicurazione? Sistema di controllo qualità rigoroso. Le apparecchiature professionali per l'analisi includono NMR, LC-MS, GC, HPLC, ICP-MS, UV, IR, OR, K.F, ROI, LOD, MP, chiarezza, solubilità, test del limite microbico, ecc.
Campioni? La maggior parte dei prodotti fornisce campioni gratuiti per la valutazione della qualità, i costi di spedizione sono a carico dei clienti.
Audit di fabbrica? Benvenuto dell'audit di fabbrica. Si prega di fissare un appuntamento in anticipo.
MOQ? Nessun MOQ. Il piccolo ordine è accettabile.
Tempi di consegna? Se disponibile in magazzino, consegna garantita in tre giorni.
Trasporti? Per espresso (FedEx, DHL), per via aerea, via mare.
Documenti? Servizio post-vendita: possono essere forniti COA, MOA, ROS, MSDS, ecc.
Sintesi personalizzata? Può fornire servizi di sintesi personalizzati per soddisfare al meglio le vostre esigenze di ricerca.
Termini di pagamento? La fattura proforma verrà inviata prima dopo la conferma dell'ordine, allegata alle nostre coordinate bancarie. Pagamento tramite T/T (trasferimento telex), PayPal, Western Union, ecc.
ID ONU UN 2811 6.1 / PGII
WGK Germania 3
RTECS FA9550000
Codice HS 29242990
Classe di pericolo 6.1
Gruppo di imballaggio III
La rivastigmina tartrato (CAS: 129101-54-8) è il tartrato della rivastigmina, un farmaco per il trattamento del morbo di Alzheimer. La rivastigmina è un derivato della fisostigmina, sviluppato per la prima volta con successo da Novartis, Svizzera. Il nome commerciale è exelon e la molecola ha una struttura benzil carbammato, è un carbammato cerebrale - inibitore selettivo della colinesterasi, che può inibire l'acetilcolinesterasi e la butirrilcolinesterasi allo stesso tempo e promuovere la conduzione del nervo colinergico ritardando la degradazione dell'acetilcolina rilasciata dai neuroni colinergici. Può migliorare la disfunzione cognitiva mediata dal colinergico, migliorando così l'effetto cognitivo dei pazienti con malattia di Alzheimer. La capacità di legame della rivastigmina con le proteine plasmatiche è debole, facile da attraversare la barriera ematoencefalica e presenta un elevato grado di selettività cerebrale. Non solo può agire selettivamente sulle aree più vulnerabili della corteccia cerebrale e dell’ippocampo, ma anche inibire preferenzialmente i sottotipi dominanti di AChE nel cervello, il che può ridurre gli effetti collaterali colinergici periferici producendo effetti curativi. L’emivita della rivastigmina tartrato nell’organismo è breve e il tempo di azione è lungo. A differenza della tacrina, questo prodotto ha un effetto inibitorio più forte sull'enzima G1 nell'ippocampo e nella corteccia. È clinicamente usato per trattare la demenza di Alzheimer da lieve a moderata, che si sospetta sia la malattia di Alzheimer o la malattia di Alzheimer.
1. Come inibitore dell'acetilcolinesterasi, la rivastigmina bicartrato può migliorare l'effetto del rilassante muscolare della succinilcolina. Pertanto, prima dell'anestesia, dovrebbe esserci un periodo intermittente adeguato per interrompere l'assunzione di questo prodotto. Questo prodotto deve essere combinato con altri preparati colinergici o anticolinergici e si deve prestare cautela (vedere [Interazioni farmacologiche]).
2. A causa dei loro effetti farmacologici, gli inibitori della colinesterasi possono avere effetti sulla tensione del nervo vago sulla frequenza cardiaca. Come con altri farmaci colinergici, è necessario prestare cautela quando viene somministrato a pazienti con sindrome del seno malato o altro blocco cardiaco (vedere Reazioni avverse).
3. L'eccitazione del nervo colinergico può causare un aumento della secrezione di acido gastrico. Sebbene durante il periodo dello studio clinico non sia stata riscontrata alcuna evidenza di un significativo peggioramento dei sintomi corrispondenti, i pazienti ad alto rischio di ulcera gastrica, come quelli con una storia di ulcera o quelli che ricevono un trattamento concomitante con farmaci antinfiammatori non steroidei, devono essere usati con cautela.
4. Come altri inibitori della colinesterasi, i pazienti con anamnesi di asma o altre malattie polmonari ostruttive devono essere usati con cautela.